Первая группа реакций реакции замещения. Мы говорили, что арены не имеют кратных связей в структуре молекулы, а содержат сопряженную систему из шести электронов, которая очень стабильна и придает дополнительную прочность бензольному кольцу. Поэтому в химических реакциях происходит в первую очередь замещение атомов водорода, а не разрушение бензольного кольца.
С реакциями замещения мы уже сталкивались при разговоре об алканах , но для них эти реакции шли по радикальному механизму, а для аренов характерен ионный механизм реакций замещения.
Первое химическое свойство галогенирование. Замещение атома водорода на атом галогена хлора или брома.
Реакция идет при нагревании и обязательно с участием катализатора. В случае с хлором это может быть хлорид алюминия или хлорид железа три. Катализатор поляризует молекулу галогена, в результате чего происходит гетеролитический разрыв связи и получаются ионы.
Положительно заряженный ион хлора и вступает в реакцию с бензолом.
Если реакция происходит с бромом, то катализатором выступает бромид железа три или бромид алюминия.

Важно отметить, что реакция происходит с молекулярным бромом, а не с бромной водой. С бромной водой бензол не реагирует.
У галогенирования гомологов бензола есть свои особенности. В молекуле толуола метильная группа облегчает замещение в кольце, реакционная способность повышается, и реакция идет в более мягких условиях, то есть уже при комнатной температуре.

Важно отметить, что замещение всегда происходит в орто- и пара-положениях, поэтому получается смесь изомеров.
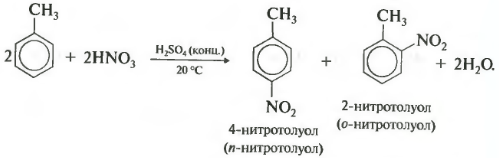
Второе свойство нитрование бензола, введение нитрогруппы в бензольное кольцо.

Образуется тяжелая желтоватая жидкость с запахом горького миндаля нитробензол, поэтому реакция может быть качественной на бензол. Для нитрования используется нитрующая смесь концентрированной азотной и серной кислот. Реакция проводится при нагревании.
Напомню, что для нитрования алканов в реакции Коновалова использовалась разбавленная азотная кислота без добавления серной.
При нитровании толуола, также как и при галогенировании, образуется смесь орто- и пара- изомеров.
Третье свойство алкилирование бензола галогеналканами.

Эта реакция позволяет ввести углеводородный радикал в бензольное кольцо и может считаться способом получения гомологов бензола. В качестве катализатора используется хлорид алюминия, способствующий распаду молекулы галогеналкана на ионы. Также необходимо нагревание.
Четвертое свойство алкилирование бензола алкенами.

Таким способом можно получить, например, кумол или же этилбензол. Катализатор хлорид алюминия.
Вторая группа реакций реакции присоединения. Мы говорили, что эти реакции не характерны, но они возможны при достаточно жестких условиях с разрушением пи-электронного облака и образованием шести сигма-связей.
Пятое свойство в общем списке гидрирование, присоединение водорода.
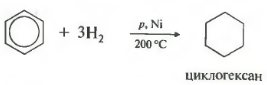
Температура, давление, катализатор никель или платина. Таким же образом способен реагировать толуол.
Шестое свойство хлорирование. Обратите внимание, что речь идет именно о взаимодействии с хлором, поскольку бром в эту реакцию не вступает.
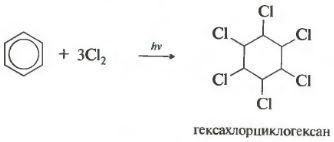
Реакция протекает при жестком ультрафиолетовом облучении. Образуется гексахлорциклогексан, другое название гексахлоран, твердое вещество.
Важно помнить, что для бензола не возможны реакции присоединения галогеноводородов (гидрогалогенирование) и присоединение воды (гидратация).
Третья группа реакций касается только гомологов бензола это замещение в боковой цепи.
Седьмое свойство в общем списке галогенирование по альфа-атому углерода в боковой цепи.

Реакция происходит при нагревании или облучении и всегда только по альфа-углероду. При продолжении галогенирования, второй атом галогена снова встанет в альфа-положение.
Четвертая группа реакций окисление.
Бензольное кольцо слишком прочное, поэтому бензол не окисляется перманганатом калия не обесцвечивает его раствор. Это очень важно помнить.
Зато гомологи бензола окисляются подкисленным раствором перманганата калия при нагревании. И это восьмое химическое свойство.

Получается бензойная кислота. Наблюдается обесцвечивание раствора. При этом, какой бы длинной не была углеродная цепь заместителя, всегда происходит ее разрыв после первого атома углерода и альфа-атом окисляется до карбоксильной группы с образованием бензойной кислоты. Оставшаяся часть молекулы окисляется до соответствующий кислоты или, если это только один атом углерода, до углекислого газа.
Если гомолог бензола имеет больше одного углеводородного заместителя у ароматического кольца, то окисление происходит по тем же правилам окисляется углерод, находящийся в альфа-положении.
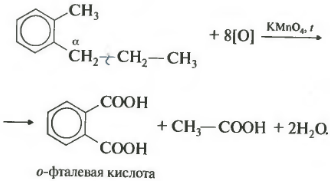
В данном примере получается двухосновная ароматическая кислота, которая называется фталевая кислота.
Особым образом отмечу окисление кумола, изопропилбензола, кислородом воздуха в присутствии серной кислоты.

Это так называемый кумольный способ получения фенола. Как правило, сталкиваться с этой реакцией приходится в вопросах, касающихся получения фенола. Это промышленный способ.
Девятое свойство горение, полное окисление кислородом. Бензол и его гомологи сгорают до углекислого газа и воды.
Запишем уравнение горения бензола в общем виде.
По закону сохранения массы атомов слева должно быть столько же, сколько атомов справа. Потому что ведь в химических реакциях атомы никуда не деваются, а просто изменяется порядок связей между ними. Так вот молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле арена, поскольку в состав молекулы входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть (2n-6)/2, а значит n-3.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа, потому что в каждой молекуле два атома кислорода, плюс n-3 из воды, итого 3n-3. Слева атомов кислорода столько же 3n-3, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть (3n-3)/2 молекул кислорода.
Таким образом, мы составили уравнение сгорания гомологов бензола в общем виде.
Гомологи бензола способны реагировать по двум направлениям с участием ароматического ядра и боковой цепи (алкильных групп) в зависимости от природы реагента.
За счёт донорного эффекта алкильной группы реакции S E ArH идут в орто - и пара -положения ароматического ядра, при этом условия мягче чем для бензола.
а) галоидирование

б) нитрование


Обратите внимание, как, по мере увеличения числа акцепторных групп (-NO 2), повышается температура реакций нитрования.
в) сульфирование

В реакции преимущественно образуется п -изомер.
г) алкилирование

д) ацилирование

Алкильный фрагмент молекулы бензола вступает в реакции S R с участием атома углерода в α -положении (бензильное положение).


Окисление всех гомологов бензола KMnO 4 /100°C приводит к образованию бензойной кислоты.
Конденсированные арены

Конденсированные арены являются ароматическими системами (n=2 и 3). Степень ароматичности конденсированных аренов ниже, чем для бензола. Для них характерны реакции электрофильного замещения, реакции присоединения и окисления, идущие в более мягких условиях, чем для бензола.
Реакционная способность нафталина
Реакции S E ArH для нафталина идут, главным образом, по α -положению, за исключением сульфирования. Электрофильное присоединение Ad E протекает по положениям 1,4, при этом нафталин проявляет свойства сопряженных диенов.
1. Реакции электрофильного замещения, S E ArH


2.Реакции электрофильного присоединения, восстановления и окисления.


Реакционная способность антрацена и фенантрена
Реакции электрофильного замещения, S E ArH и электрофильного присоединения, Ad E для антрацена протекают преимущественно по положениям 9 и 10 (см. нижеприведенную схему).

Реакции электрофильного замещения, S E ArH и электрофильного присоединения, Ad E для фенантрена протекают преимущественно по положениям 9 и 10, как и для антрацена (см. ниже приведенную схему).

Реакции окисления и восстановления для антрацена и фенантрена.


Структуры некоторых лекарственных препаратов на основе нафталина, антрацена и фенантрена
Нафтизин (нафазолин, санорин)

сосудосуживающее действие (лечение ринитов, синуситов)
(в названии подчеркнута родоначальная структура, обратите внимание на нумерацию)
Нафтифин

противогрибковое действие (лечение дерматитов)
Набуметон

противовоспалительное, жаропонижающее, анальгезирующее действие (лечение остеоартрита, ревматоидного артрита).
Надолол

(термин цис, в данном случае, обозначает взаимное расположение гидроксильных групп)
гипотензивное (понижает артериальное давление) и антиаритмическое действие
Морфин, кодеин

Контрольные вопросы к главе «АРЕНЫ»
1. Какие свойства бензола отличают его от других ненасыщенных соединений-алкенов, алкинов? Что означает термин “ароматическое соединение”?
2. Напишите структурные формулы соединений: а) этилбензола; б) 1,3-диметилбензола (м -ксилола); в) 1,3,5-триметилбензола (мезитилена); г) изопропилбензола (кумола); д) 3-фенилпентана; е) винилбензола (стирола); ж) фенилацетилена; з)транс -дифенилэтилена (транс -стильбена).
3. Охарактеризуйте особенности строения соединений, проявляющих ароматичность. Сформулируйте правило Хюккеля. Какие из приведенных ниже соединений являются ароматическими:

4. Сравните отношение циклогексена и бензола к следующим реагентам в указанных условиях: а) Br 2 (H 2 O, 20 C); б) KMnO 4 (H 2 O, 0 C); в) Н 2 SO 4 (конц.) , 20 C; г) H 2 (Pd, 30 C); д) О 3 , затем H 2 O (Zn); е) HBr.
5. Напишите структурные формулы монозамещенных бензола, образующихся в реакциях бензола со следующими реагентами: а) Н 2 SO 4 (конц.); б) HNO 3 ; Н 2 SO 4 (конц.); в) Br 2 /Fe; г) Cl 2 /AlCl 3 ; д) СН 3 Br/AlBr 3 ; e) СН 3 COCl/AlСl 3 . Назовите реакции и их продукты. Укажите, с каким электрофилом реагирует бензол в каждом конкретном случае.
6. Приведите общую схему взаимодействия бензола с электрофильным реагентом (Е + ). Назовите промежуточные комплексы. Какая стадия обычно определяет скорость реакции? Приведите график изменения потенциальной энергии рассматриваемой реакции.
7. Дайте определение следующим понятиям: а) переходное состояние; б) промежуточное соединение; в) -комплекс; г)-комплекс. Какие из них являются тождественными? Проиллюстрируйте эти понятия на примере бромирования бензола в присутствии катализатораFeBr 3 .
8. На примере реакций этена и бензола с бромом сравните механизм электрофильного присоединения у алкенов с механизмом электрофильного замещения в ароматическом ряду. На какой стадии наблюдается различие и почему?
9. С помощью индуктивных и мезомерных эффектов опишите взаимодействие заместителя с бензольном кольцом в указанных соединениях:

Отметьте электронодонорные (ЭД) и электроноакцепторные (ЭА) заместители.
10. Напишите схемы мононитрования соединений: а) фенола; б) бензолсульфокислоты; в) изопропилбензола; г) хлорбензола. Для какого соединения относительная скорость замещения должна быть наибольшей и почему?
11. Образование каких продуктов следует ожидать при моносульфировании соединений: а) толуола; б) нитробензола; в) бензойной кислоты; г) бромбензола? Какое соединение должно сульфироваться легче всех? Почему?
12. Следующие соединения расположите в ряд по увеличению реакционной способности при бромировании их в бензольное кольцо: а) бензол; б) фенол; в) бензальдегид; г) этилбензол. Дайте объяснения.
13. Назовите следующие углеводороды:

14. Напишите реакции бензола со следующими реагентами: а) Cl 2 (Fe); б) 3Cl 2 (свет); в) HNO 3 (H 2 SO 4 ); г) О 2 (воздух) (V 2 О 5 , 450 C); д) 3О 3 , затем Н 2 О (Zn); е) H 2 SO 4 (олеум); ж) 3Н 2 (Ni, 200 C, p ). В чем состоит особенность реакций присоединения у бензола?
15. Напишите реакции толуола с указанными реагентами: а) 3Н 2 (Ni, 200 C, 9806,7 кПа); б) KMnO 4 в Н 2 О; в*) Сl 2 , свет; г*) Cl 2 (Fe); д*) СН 3 Cl (AlCl 3 ); e*) СН 3 COCl (AlCl 3 ); ж) HNO 3 (H 2 SO 4 ). Для реакций, отмеченных звездочкой, приведите механизмы.
16. Напишите реакции нитрования этилбензола в указанных условиях: а) 65% HNO 3 + H 2 SO 4 (конц.); б) 10% HNO 3 , нагревание, давление. Приведите механизмы.
17. Сравните отношение изопропилбензола к брому: а) в присутствии AlBr 3 ; б) при освещении и нагревании. Приведите реакции и их механизмы.
18. Какие соединения образуются из этилбензола и п -ксилола при действии указанных окислителей:а) О 3 , затем H 2 О (Zn); б) КMnO 4 в H 2 О, t ; в) К 2 Cr 2 O 7 в H 2 SО 4 , t ?
19. С помощью каких реакций можно различить следующие пары соединений: а) этилбензол и м -ксилол; б) этилбензол и стирол; в) стирол и фенилацетилен; г)о - ип -ксилолы?
20. Какие соединения являются продуктами приведенных ниже реакций:

21. Исходя из бензола и любых других реагентов, получите приведенные ниже соединения: а) п -трет -бутилтолуол; б) этил-п -толилкетон; в) алилбензол; г)п -бромбензойную кислоту.
22. Назовите главные соединения, образующиеся в следующих реакциях:

Таким соединением, как бензол, госпожа Химия в своем хозяйстве окончательно и бесповоротно обзавелась только в 1833 году. Бензол - это соединение, которое имеет вспыльчивый, можно сказать, даже взрывной характер. Как это выяснили?
Иоган Глаубер в 1649 году обратил свое внимание на соединение, которое благополучно образовалось, когда химик занимался обработкой каменноугольной смолы. Но оно пожелало остаться инкогнито.
Спустя около 170 лет, а если быть гораздо более точным, в середине двадцатых годов XIX века, по воле случая из светильного газа, а именно из выделившегося конденсата, извлекли бензол. Таким стараниям человечество обязано Майклу Фарадею, ученому из Англии.
Эстафету по приобретению бензола перехватил немец Эйльгард Мичерлих. Это случилось, когда проходил процесс обработки безводных солей кальция бензойной кислоты. Возможно, поэтому соединению дали такое наименование - бензол. Еще, как вариант, ученый называл его бензином. Благовоние, если в переводе с арабского.
Бензол красиво и ярко горит, в связи с этими наблюдениями Огюст Лоран посоветовал назвать его «фен» или «бензен». Яркий, блистающий - если перевести с греческого языка.
Опираясь на мнение понятие о природе электронной связи, о качествах бензола, ученый предоставил молекулу соединения в виде следующего образа. Это шестиугольник. В него вписана окружность. Вышесказанное говорит о том, что у бензола целостное электронное облако, которое благополучно заключает шесть (без исключения) атомов углерода цикла. Скрепленных бинарных связей не наблюдается.
С бензолом раньше работали как с растворителем. А в основном, как говорится, не состоял, не участвовал, не привлекался. Но это в XIX веке. В XX произошли существенные перемены. Свойства бензола выражают ценнейшие качества, которые помогли ему стать более популярным. Октановое число, которое оказалось высоким, предоставило возможность применять его в качестве элемента топлива для заправки автомобилей. Сие действо послужило толчком обширного изъятия бензола, добыча оного осуществляется как вторичный продукт коксования изготовления стали.
К сороковым годам в химической сфере бензол начал потребляться в изготовлении веществ, которые быстро взрываются. XX век увенчал себя тем, что нефтеперерабатывающая промышленность выработала бензола столько, что стала снабжать химическую индустрию.
Ненасыщенные углеводороды очень схожи с бензолом. Например, углеводородный ряд этилена характеризует себя как ненасыщенный углеводород. Ему свойственна реакция присоединения. Бензол охотно вступает в Все это благодаря атомам, которые находятся в одной плоскости. И как факт - сопряженное электронное облако.

Если в формуле присутствует бензольное кольцо, значит, можно прийти к элементарному выводу, что это - бензол, структурная формула которого выглядит именно так.
Бензол - это жидкость которая не имеет цвета, зато имеет достойный сожаления запах. Плавится бензол, когда температура достигает 5,52 градусов по Цельсию. Кипит при 80,1. Плотность составляет 0,879 г/см 3 , масса молярная равна 78,11 г/моль. При горении сильно коптит. Формирует взрывоопасные соединения, когда проникает воздух. породы (бензин, эфир и прочие) с описываемым веществом соединяются без проблем. Азеотропное соединение создает с водой. Нагрев до начала парообразования происходит при 69,25 градусов (91 % бензола). При 25 градусах по Цельсию может растворяться в воде 1,79 г/л.
Бензол реагирует с серной и азотной кислотой. А также с алкенами, галогенами, хлоралканами. Реакция замещения - вот что ему свойственно. Температура давления влияет на прорыв кольца бензола, которое проходит в достаточно резких условиях.
Каждое уравнение реакции бензола мы можем рассмотреть более детально.
1. Электрофильное замещение. Бром, при наличии катализатора, взаимодействует с хлором. В результате получаем хлоробензол:
С6H6+3Cl2 → C6H5Cl + HCl
2. Реакция Фриделя-Крафтса, или алкилирование бензола. Появление алкилбензолов происходит благодаря соединению с алканами, которые являются галогенопроизводными:
C6H6 + C2H5Br → C6H5C2H5 + HBr
3. Электрофильное замещение. Здесь идет реакция нитрования и сульфирования. Выглядеть уравнение бензола будет следующим образом:
C6H6 + H2SO4 → C6H5SO3H + H2O
C6H6 + HNO3 → C6H5NO2 + H2O
4. Бензол при горении:
2C6H6 + 15O2 → 12CO2 + 6H2O
При определенных условиях проявляет характер, свойственный насыщенным углеводородам. П-электронное облако, которое находится в строении рассматриваемого вещества, объясняет эти реакции.
От спецтехнологии зависят различные виды бензола. Отсюда происходит маркировка нефтяного бензола. Например, очищенный и высшей очистки, для синтеза. Хотелось бы отдельно отметить гомологи бензола, а если конкретнее - их химические свойства. Это алкилбензолы.

Гомологи бензола гораздо охотнее реагируют. Но вышесказанные реакции бензола, а именно гомологов, проходят с некоторым отличием.
Вид уравнения следующий:
С6H5-CH3 + Br = C6H5-CH2Br + HBr.
Стремление брома в кольцо бензола не наблюдается. Он выходит в цепочку сбоку. Зато благодаря катализатору соли Al(+3) бром смело идет в кольцо.
Благодаря серной и азотной кислотам нитрируются бензолы и алкилбензолы. Реакционноспособные алкилбензолы. Получаются два продукта из представленных трех - это пара- и орто-изомеры. Можно записать одну из формул:
C6H5 - CH3 + 3HNO3 → C6H2CH3 (NO2)3.
Для бензола это неприемлемо. Зато алкилбензолы реагируют охотно. Например, бензойная кислота. Формула приведена ниже:
C6H5CH3 + [O] → C6H5COOH.
В присутствии усилителя водород начинает реагировать с бензолом, вследствие чего образуется циклогексан, как об этом говорилось выше. Подобным образом алкибензолы без проблем преобразуются в алкилциклогексаны. Для получения алкилциклогексана требуется подвергнуть гидрированию нужный алкилбензол. В основном это необходимая процедура для производства беспримесного продукта. И это далеко не все реакции бензола и алкилбензола.
Фундамент такого производства зиждется на том, чтобы переработать составляющие: толуола, нафты, смолы, которая выделяется при крекинге угля, и прочих. Посему бензол производится на нефтехимических, металлургических предприятиях. Важно знать, как получить бензол разной степени очистки, ведь от принципа изготовления и предназначения следует прямая зависимость марки данного вещества.
Львиную долю изготавливают термокаталитическим реформингом каустобиолитной части, выкипающей при 65 градусах, обладающей эффектом экстракта, дистилляции с диметилформамидом.
При выработке этилена и пропилена получают жидкие продукты, которые образуются в ходе распада неорганических и органических соединений под воздействием тепла. Из них и выделяют бензол. Но, к сожалению, исходного материала для этого варианта добычи бензола не так уж и много. Потому интересующее нас вещество добывают риформингом. Посредством такого способа объем бензола увеличивается.

Путем деалкилирования при температуре 610-830 градусов со знаком плюс, при наличии пара, образующегося при кипении воды и водорода, из толуола получают бензол. Есть еще вариант - каталитический. Когда наблюдается наличие цеолитов, или, как вариант, катализаторов оксидных, при соблюдении температурного режима 227-627 градусов.
Существует еще один, более старый, способ разработки бензола. С помощью абсорбции поглотителями органического происхождения его выделяют из конечного результата коксования каменного угля. Продукт парогазовый и заранее подвергся охлаждению. Например, в ход пускается масло, источником которого является нефть или каменный уголь. Когда перегонка осуществляется с водяным паром, поглотитель отделяется. Гидроочистка помогает сырой бензол освободить от лишних веществ.
В металлургии при использовании каменного угля, а если уточнить - его сухой перегонки, получают кокс. Во время этой процедуры ограничивается поступление воздуха. Не стоит забывать и то, что до температуры 1200-1500 по Цельсию нагревается уголь.
Углехимический бензол нуждается в доскональном очищении. Нужно избавиться в обязательном порядке от метила циклогексана и его товарища н-гептана. тоже должны быть изъяты. Бензолу предстоит процесс разделения, очищения, который будет осуществляться не один раз.
Метод, описанный выше, самый старый, но по истечении времени он теряет свои высокие позиции.
0,3-1,2 % - такие показатели состава нашего героя в необработанной нефти. Мизерные показатели, чтобы вкладывать финансы и силы. Лучше всего задействовать промышленную процедуру по переработке нефтяных фракций. То есть каталитический риформинг. При наличии алюмо-платино-рениевого усилителя растет процент вмещения ароматических углеводов, и возрастает показатель, определяющий возможности топлива не самовозгораться при его сжатии.
Если добывать наш нефтепродукт из не твердого сырья, а именно путем пиролиза возникающих при изготовлении пропилена и этилена, то сей подход окажется наиболее приемлемым. Если быть точным, бензол выделяется из пироконденсата. Разложение определенных долей нуждается в гидроочистке. При очистке отстраняются сернистые и непредельные смеси. В исходном результате замечено содержание ксилола, толуола, бензола. С помощью перегона, который является экстактивным, БТК-группа разделяется и получается бензол.

Главные герои процесса, коктейль из водородного потока и толуола, подаются нагретыми в реактор. Толуол проходит через пласт катализатора. Во время этого процесса метильная группа отделяется с формированием бензола. Здесь уместен определенный способ очищения. Результатом становится высокочистое вещество (для нитрования).
В следствии отторжения метильного класса совершается созидание до бензола, окисляется ксилол. В данном процессе было замечено переалкилирование. Действие катализации происходит благодаря палладию, платине и неодиму, которые находятся на оксиде алюминия.
В реактор со стойким пластом катализатора подается талуол и водород. Его цель - удержать оседание на плоскость катализатора углеводородов. Поток, который выходит из реактора, подвергается охлаждению, а на рецикл благополучно извлекается водород. То, что осталось, перегоняется трижды. На начальной стадии изымаются соединения, которые являются неароматическими. Вторым добывается бензол, и последний шаг - это выделение ксилолов.
Благодаря трудам французского физико-химика Марселена Бертло из ацетилена стали изготавливать бензол. Но при этом выделялся тяжелый коктейль из многих других элементов. Стоял вопрос, как понизить температуру реакции. Ответ был получен лишь в конце сороковых годов XX века. В. Реппе нашёл соответствующий катализатор, им оказался никель. Тримеризация - это единственный вариант обрести из ацетилена бензол.

Образование бензола происходит с помощью активированного угля. При больших показателях теплоты над углем проходит ацетилен. Бензол выделяется, если температура составляет не менее 410 градусов. При этом еще рождаются разнообразные ароматические углеводороды. Поэтому необходима хорошая аппаратура, которая способна качественно очистить ацетилен. При таком трудоемком способе, как тримеризация, ацетилена расходуется очень много. Чтобы получить 15 мл бензола, берется 20 литров ацетилена. Можно просмотреть, как это выглядит в реакция не заставит себя долго ждать.
3C2H2 → C6H6 (уравнение Зелинского).
3CH → CH = (t, kat) = C6H6.
Бензол — это достаточно популярное детище химии. Особенно часто было замечено, как бензол принимали на вооружение в изготовлении кумола, циклогексана, этилбензола. Для создания стирола без этилбензола не обойтись. Исходным материалом для того, чтобы выработать капролактам, служит циклогексан. Изготавливая термопластичную смолу, применяют именно капролактам. Описываемое вещество незаменимо при изготовлении разных красок, лаков.
Бензол - это токсичное вещество. Проявление ощущения недомогания, которое сопровождается тошнотой и сильным головокружением - это признак отравления. Не исключается даже летальный исход. Чувство неописуемого восторга - это не менее тревожные звоночки при отравлении бензолом.
Бензол в жидком состоянии вызывает раздражение кожи. Бензольные пары с легкостью проникают даже через неповрежденный кожный покров. При самых недолгосрочных контактах с веществом в небольшой дозе, но на регулярной основе, неприятные последствия не заставят себя долго ждать. Это может быть поражение костного мозга и лейкозы острого характера разного вида.

Ко всему прочему, вещество вызывает зависимость у человека. Бензол действует как дурман. Из табачного дыма получается дегтеобразный продукт. Кода его изучили, то пришли к выводу, что содержание последнего небезопасно для человека. Обнаружилось помимо присутствия никотина еще и наличие ароматических углеводов вида бензпирена. Отличительной чертой бензпирена являются канцерогенные вещества. Действие они оказывают очень вредное. Например, вызывают онкологические заболевания.
Несмотря на вышесказанное, бензол является стартовым сырьем для производства разнообразных лекарственных препаратов, пластмасс, резины синтетического происхождения и, конечно же, красителей. Это самое распространённое детище химии и ароматическое соединение.
ЗаголовокПростой углеводород. Относится к ароматическим углеводородам, классу органических веществ.
Вещество представляет собой прозрачную жидкость, не имеет цвета, обладает сладковатым характерным запахом. Бензол относят к ненасыщенным углеводородам. Знаменитая формула бензольного кольца была предложена нобелевским лауреатом в области химии – Лайнусом Полингом. Именно он предложил изображать бензол в виде шестигранника с окружностью внутри. Это изображение дает понимание об отсутствии двойных связей и наличии единого электронного облака, в которое охвачены все 6 атомов углерода.
Формула
Естественный источник для получения бензола – это каменный уголь. Процесс коксования каменного угля был открыт Майклом Фарадеем в далеком 1825 году. Он изучал светильный газ, который использовали в фонарях уличного освещения, смог выделить и описать бензол. Сейчас этим способом из каменноугольной смолы бензол практически не получают. Существует множество других более продуктивных способов его получения.
3С 2 Н 2 → С 6 H 6 .
При горении выделяется большое количество копоти, так как углеводород ненасыщенный (ему не хватает 8 атомов водорода, чтобы отвечать стандартной формуле предельных углеводородов). При низких температурах бензол становится белой кристаллической массой.
Бензол вступает в реакции замещения в присутствии катализаторов – обычно это соли Al(3+) или Fe(3+):
C 6 H 6 + Br 2 = C 6 H 5 Br + HBr.
C 6 H 6 + HO-NO 2 → C 6 H 5 NO 2 + H 2 O.
С 6 H 6 + С 2 H 5 Cl → C 6 H 5 C 2 H 5 + HCl.
Гомологи бензола, содержащие радикал, реагирует не так как сам бензол. Реакции идут по-другому и часто на свету:
Реакции окисления бензола идут очень сложно и не характерны для этого вещества. Окисление характерно для гомологов. Вот, например, реакция получения бензойной кислоты:
С 6 H 5 CH 3 + [O] → C 6 H 5 COOH.
Процесс горения вещества происходит по стандартной схеме для всех органических веществ:
C n H 2n-6 + (3n-3)\2 O 2 → nCO 2 + (n-3)H 2 O.
Реакции гидрирования. Реакция проходит сложно, требуются катализаторы, давление, температура. В реакциях бензола с водородом получается циклогексан:
С 6 H 6 + 3H 2 → C 6 H 12 .
А в реакциях с алкилбензолом – метилциклогексан, где один атом водорода замещается на радикальную группу -CH 3:
С 6 H 5 CH 3 + 3H 2 → C 6 H 11 -CH 3 .
Бензол в чистом виде практически не используется. Его вырабатывают для производства других важных соединений, таких как, например, этилбензол, из которого получают стирол и полистирол.
Львиную долю бензола пускают на производства фенола, который необходим в производстве капрона, красителей, пестицидов, лекарств. Знаменитое лекарство аспирин невозможно получать без участия фенола.
Циклогексан из бензола необходим для производства пластмасс и искусственных волокон, нитробензол идет на выработку анилина, который используют для производства каучуков, красителей и гербицидов.